僄傾乕僐儞僾儗僢僒乕愱栧揦偱偡丅僐儞僾儗僢僒偺帠側傜偍擟偣偔偩偝偄両両
儃僀儖僔儍儖儖偺朄懃
嬻婥埑偱婎杮偲側傞丅儃僀儖僔儍儖儖偺朄懃偱偡偑丄僱僢僩忋傪尒搉偟偰傕娙扨側婰弎偺僒僀僩偐愱栧梡岅偑堦攖偺擄偟偄僒僀僩偟偐側偄堊丄夝傝傗偡偔妿偮徻偟偔愢柧偄偨偟傑偡丅
乮侾乯嬻婥偺忬懺曄壔
婥懱偵偼丄埑椡丒懱愊丒壏搙偺嶰梫慺偱堦掕偺娭學偑偁傝丄偙偺偆偪俀梫慺偑寛傑傟偽巆傝偺侾梫慺偼昁慠揑偵寛掕偝傟傑偡丅嬻婥偺応崌偵傕俁梫慺偱昞偣嶰梫慺娫偺娭學傪昞偡幃傪乽忬懺幃乿偲偄偄傑偡丅
忬懺偺曄壔偼乽摍壏曄壔乿乽抐擬曄壔乿偵戝暿偝傟丄嬻婥偲奜晹偲偺擬偺弌擖傝偑帺桼側忬懺偱偺曄壔傪乽摍壏曄壔乿丄擬偺弌擖傝偑慡偔側偄忬懺偱偺曄壔傪乽抐擬曄壔乿偲偄偄傑偡丅
乮俀乯儃僀儖偺朄懃
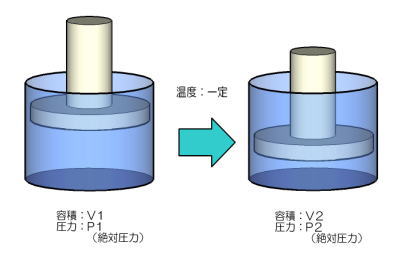
埑椡媦傃懱愊偑堦掕検偺嬻婥傪壏搙傪曐偭偨傑傑埑弅傑偨偼朿挘偝偣偨応崌丅師偺幃偑惉傝棫偪傑偡丅
曄壔慜偺埑椡亊曄壔慜偺懱愊亖曄壔屻偺埑椡亊曄壔屻偺懱愊
俹侾亊倁侾亖俹俀亊倁俀
壏搙偑堦掕偱偁傟偽丄堦掕検偺婥懱偺埑椡偲懱愊偺愊偼忢偵堦掕偱偁傝丄偙傟傪乽儃僀儖偺朄懃乿偲偄偄傑偡丅
乮俁乯僔儍儖儖偺朄懃
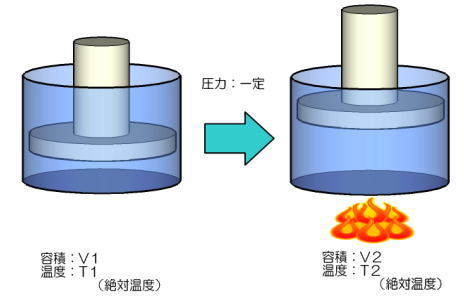
懱愊媦傃愨懳壏搙偑堦掕検偺嬻婥偺埑椡傪堦掕偵曐偭偨傑傑壛擬傑偨偼椻媝偝偣偨応崌丄師偺幃偑惉傝棫偪傑偡丅
| 曄壔慜偺愨懳壏搙 | 亖 | 曄壔慜偺懱愊 |
| 曄壔屻偺愨懳壏搙 | 曄壔屻偺懱愊 |
| 俿侾 | 亖 | 倁侾 |
| 俿俀 | 倁俀 |
埑椡偑堦掕偱偁傟偽丄堦掕検偺嬻婥偺懱愊偼愨懳壏搙偵惓斾椺偺娭學偱偁傝丄偙傟傪乽僔儍儖儖偺朄懃乿偲偄偄傑偡丅
乮係乯儃僀儖丒僔儍儖儖偺朄懃
堦掕検偺婥懱偺埑椡傗壏搙傪曄偊傞偲懱愊偑曄傢傞偙偲偼乽儃僀儖偺朄懃乿偲乽僔儍儖儖偺朄懃乿偐傜抦傞偙偲偑弌棃傞偑丄埑椡丄壏搙丄懱愊偺嶰梫慺偑嫟偵曄壔偡傞応崌丄偙傟傜俀偮偺朄懃傪侾偮偵傑偲傔偨傕偺偑昁梫偲側傝丄偙傟偑乽儃僀儖丒僔儍儖儖偺朄懃乿偲側傝傑偡丅
埑椡亊懱愊亖婥懱偺廳検亊僈僗忢悢亊愨懳壏搙
俹倁亖俧俼俿
乽僈僗忢悢乿偼婥懱偺庬椶偵傛傝掕傑傞悢抣偱嬻婥偺応崌偼俀俋丏俈kgf/kgf偱偁傞丅
偙偺幃傪乽忬懺幃乿傗乽儃僀儖丒僔儍儖儖偺幃乿偲偄偄傑偡丅
乮俆乯摍壏曄壔偺応崌
堦掕検偺婥懱偺忬懺曄壔偑堦掕壏搙偺傕偲峴傢傟傞曄壔傪乽摍壏曄壔乿偲偄偄埑椡偲懱愊偑堦掕検偺婜懸偑壏搙曄壔柍偟偵曄壔偡傞応崌乽儃僀儖丒僔儍儖儖偺朄懃乿偐傜師偺幃偑惉傝棫偪傑偡丅
俹侾亊倁侾亖俧亊俼亊俿
俹俀亊倁俀亖俧亊俼亊俿
偲側傝
俹侾乛俹俀亖倁俀乛倁侾
偺娭學偑惉傝棫偪傑偡丅
埑椡偼懱愊偵斀斾椺偡傞偙偲偑徹柧偝傟傑偡丅偙傟偼乽儃僀儖偺朄懃乿偦偺傕偺偱偁傝壏搙曄壔傪敽偆応崌偵傕摨條偵偟偰師偺幃偑惉傝棫偪傑偡丅
俹侾亊倁侾亖俧亊俼亊俿侾
俹俀亊倁俀亖俧亊俼亊俿俀
偲側傝
| 俹侾亊倁侾 | 亖 | 俹俀亊倁俀 |
| 俿侾 | 俿俀 |
乮俇乯抐擬曄壔偺応崌
堦掕検偺婥懱偑奜晹偲偺擬偺弌擖傝偑慡偔側偄忬懺偱埑椡傗懱愊偑曄壔偡傞偙偲傪乽抐擬曄壔乿偲偄偄丄婥懱偑朿挘偟懱愊偑憹壛偡傟偽丄奜晹偵懳偟偰巇帠傪偟偨偙偲偵側傞偑丄奜晹偲偺擬偺弌擖傝偑側偄忬懺偱峴傢傟傞偲婥懱偺帩偮僄僱儖僊乕偺堦晹偑徚旓偝傟丄婥懱偺壏搙偑掅壓偟乽摍壏曄壔乿偺応崌偵斾傋埑椡偼掅偔側傝傑偡丅
媡偵埑弅偝傟懱愊偑尭彮偡傞偲僄僱儖僊乕偑婥懱偺撪晹偵拁偊傜傟偨偙偲偵側傝丄乽摍壏曄壔乿偵斾傋埑椡偺曄壔偼戝偒偔側傝傑偡丅
堦斒揑偵僄傾乕僐儞僾儗僢僒偱偺嬻婥傪埑弅偡傞応崌傗丄僄傾乕僞儞僋偵拁偊傜傟偨嬻婥傪堦婥偵曻弌偡傞応崌偼曄壔偑抁帪娫偱峴傢傟傞偨傔乽抐擬曄壔乿偲傒側偟傑偡丅
抐擬曄壔偺応崌偺埑椡偺懱愊偼師偺幃偱昞偣傑偡丅
埑椡亊斾梕愊亊抐擬斾亖堦掕
俹亊倴亊倠亖堦掕
| 斾梕愊倴丗 | 侾 | ||
| 乮 | 俹 | 乯 | |
| 俼俿 |
| 抐擬斾倠丗 | 掕埑斾擬 |
| 掕愊斾擬 |
偱偁傝
俹侾亊倴侾亊倠亖俹俀亊倴俀亊倠
偲側傝傑偡丅
抐擬斾倠偼抐擬曄壔傪昞偡巜悢偱乽抐擬巜悢乿偲傕偄偄丄嬻婥偺応崌偼侾丏係偲側傝傑偡丅壏搙偲偺娭學幃偼乽僔儍儖儖偺朄懃乿偐傜師偺幃偱昞偣傑偡丅
| 俿侾 | 亖 | 乮 | 俹侾 | 乯 | k-1 k |
亖 | 乮 | 倴俀 | 乯 | k-1 | |
| 俿俀 | 俹俀 | 倴侾 | |||||||||